Breve Resumen
Este video explora las propiedades únicas del agua y su importancia para la vida. Se centra en la estructura molecular del agua, los enlaces de hidrógeno, las propiedades físico-químicas, la solubilidad de sustancias en agua, las soluciones, la osmolaridad y la presión osmótica.
- La estructura molecular del agua y su capacidad para formar enlaces de hidrógeno son clave para sus propiedades únicas.
- El agua actúa como solvente universal y es esencial para la termorregulación y la homeostasis.
- La osmolaridad y la presión osmótica son cruciales para entender el comportamiento de las células en diferentes soluciones.
Introducción
Dolores Piñero, docente de bioquímica, presenta una clase sobre agua y soluciones, enfocándose en las características moleculares del agua que la hacen esencial para la vida. Se explorarán la estructura de la molécula de agua, sus propiedades especiales, la formación de enlaces de hidrógeno y cómo estas propiedades la convierten en un solvente universal. También se abordará la solubilidad de diferentes sustancias en agua, la concentración de soluciones y la importancia de la presión osmótica.
Estructura de la Molécula de Agua
La molécula de agua está compuesta por un átomo de oxígeno y dos átomos de hidrógeno unidos por enlaces covalentes simples. La disposición espacial de la molécula es tetraédrica, con el oxígeno en un vértice y los hidrógenos abiertos. El oxígeno, al ser electronegativo, atrae los electrones del enlace, adquiriendo una carga parcial negativa, mientras que los hidrógenos adquieren cargas parciales positivas. Esta distribución de cargas convierte al agua en un dipolo, aunque su carga neta sea cero.
Enlace de Hidrógeno
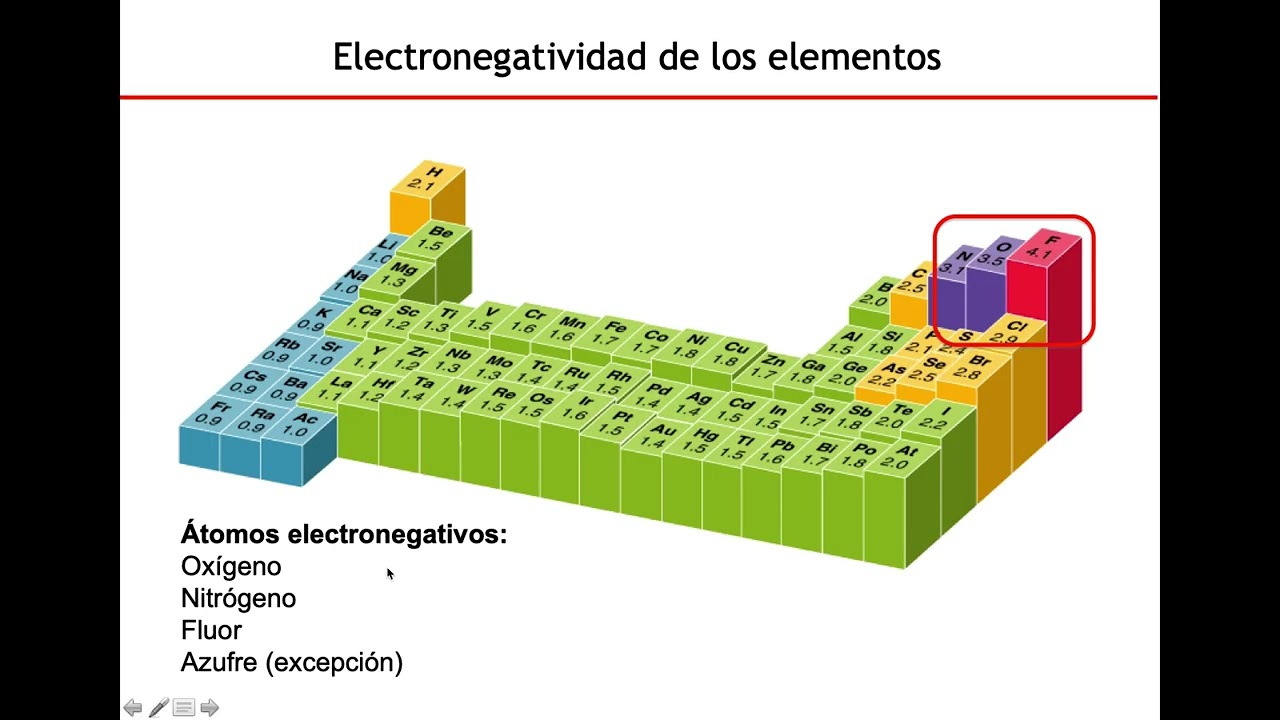
El enlace de hidrógeno es una interacción electrostática entre un átomo electronegativo (oxígeno, nitrógeno, flúor) y un átomo de hidrógeno unido covalentemente a otro átomo electronegativo. Es un enlace débil, pero el gran número de enlaces de hidrógeno en el agua le confiere una gran cohesión interna. Cada molécula de agua puede formar hasta cuatro puentes de hidrógeno, lo que se observa en la estructura ordenada del hielo.
Propiedades Físico-Químicas del Agua
La capacidad del agua para formar enlaces de hidrógeno le otorga una alta cohesión interna, lo que resulta en un alto punto de fusión, ebullición y calor específico. Comparada con moléculas de peso molecular similar, el agua presenta valores superiores en estas propiedades. Su densidad máxima a 4 grados Celsius permite que el hielo flote, esencial para la vida acuática en climas fríos. Además, el agua se disocia en una pequeña proporción, generando iones de hidrógeno que definen el concepto de pH.
Solubilidad de los Elementos
La solubilidad de los elementos en agua depende de su capacidad para interaccionar con ella. Los compuestos polares o cargados, que pueden formar enlaces de hidrógeno con el agua, son hidrofílicos y tienen alta solubilidad. Los compuestos apolares, que no pueden formar enlaces de hidrógeno, son hidrofóbicos y tienen baja solubilidad. Algunas moléculas son anfipáticas, con regiones hidrofílicas e hidrofóbicas.
Tipos de Solutos y Formación de Puentes de Hidrógeno
Las sustancias polares presentan dipolos o cargas parciales, mientras que las apolares no. Para que una sustancia forme puentes de hidrógeno con el agua, debe ser una molécula cargada o tener cargas parciales. Los átomos electronegativos como el oxígeno y el nitrógeno actúan como aceptores de hidrógeno, mientras que los átomos de hidrógeno unidos a átomos electronegativos actúan como dadores.
Interacciones No Covalentes
Además de los enlaces de hidrógeno, existen otras interacciones no covalentes importantes, como las interacciones dipolo-dipolo, iónicas, ion-dipolo, fuerzas de Van der Waals e interacciones hidrofóbicas. Las interacciones iónicas implican la transferencia de electrones entre átomos, resultando en la formación de iones con cargas opuestas.
Interacciones Hidrofóbicas
Las interacciones hidrofóbicas ocurren entre moléculas apolares en agua. Estas moléculas tienden a unirse para minimizar su contacto con el agua, formando estructuras como micelas, donde las cabezas polares interactúan con el agua y las colas apolares se esconden en el interior.
Moléculas Polares, No Polares y Anfipáticas
Las moléculas polares contienen grupos funcionales como hidroxilos (-OH), carbonilos (C=O) o aminos (-NH2), que pueden formar enlaces de hidrógeno con el agua. Las moléculas no polares están formadas principalmente por carbono e hidrógeno y no pueden interaccionar con el agua. Las moléculas anfipáticas tienen regiones polares y no polares.
Soluciones
Las soluciones son sistemas homogéneos formados por un solvente y un soluto. Para definir una solución, es necesario conocer su naturaleza química y su concentración, que se puede expresar en unidades físicas (porcentaje masa/volumen, volumen/volumen, masa/masa, gramos por litro) o químicas (molaridad, normalidad, osmolaridad).
Osmolaridad y Presión Osmótica
La osmolaridad es un concepto clave en biología, relacionado con el movimiento de agua a través de membranas semipermeables. La ósmosis es el movimiento de agua desde una solución menos concentrada a una más concentrada, buscando igualar las concentraciones. Las soluciones isotónicas tienen la misma osmolaridad, mientras que las hipertónicas e hipotónicas tienen mayor o menor osmolaridad, respectivamente.
Cálculo de la Osmolaridad
La osmolaridad se calcula relacionando la molaridad con el número de partículas en solución. En soluciones no iónicas, el número de partículas coincide con el número de moles. En soluciones iónicas, cada molécula se disocia en dos o más iones. La osmolaridad normal del plasma es de aproximadamente 310 miliosmoles.
Presión Osmótica e Importancia Biológica
La presión osmótica es la fuerza necesaria para contrarrestar el movimiento de agua a través de una membrana semipermeable. Si las células se colocan en soluciones con diferente osmolaridad, pueden experimentar cambios en su volumen. En soluciones isotónicas, no hay movimiento neto de agua. En soluciones hipertónicas, el agua sale de la célula, causando crenación. En soluciones hipotónicas, el agua entra en la célula, causando lisis.
Composición de los Fluidos Corporales
La osmolaridad de los fluidos corporales es el resultado de la suma de electrolitos y no electrolitos. Existe una diferencia en la composición entre el líquido extracelular (rico en sodio y cloruro) y el líquido intracelular (rico en potasio y fosfatos). El organismo mantiene una presión osmótica casi constante en todos sus compartimentos, y los cambios en la concentración de solutos pueden tener repercusiones en la distribución del agua.
Resumen de la Clase
Se revisaron la estructura molecular del agua, su capacidad para formar enlaces de hidrógeno, sus propiedades excepcionales, la solubilidad de sustancias en agua, las interacciones hidrofóbicas, las soluciones, la osmolaridad y la presión osmótica. Se destacó la importancia de estos conceptos en biología y medicina.